



 有临
有临
 2022.10.20
2022.10.20
 4402
4402
从20世纪70年代L.B. Sheiner等人提出了群体药代动力学(population pharmacokinetics,PopPK)的概念至今,PopPK已广泛地用于指导新药研发。早在1999年美国食品药品监督管理局(FDA)发布《群体药代动力学制药工业指南》,我国CDE也已在2020年发布首个PopPK指导原则,为新药申请(NDAs)、生物制剂许可申请(BLA)等过程中应用PopPK分析做出规范和指导。
01 PopPK原理
经典的药代动力学(pharmacokinetics,PK)分析,往往无法解释个体内、个体间差异的类型、程度及原因。PopPK方法将更多潜在的影响PK特征的因素(性别、年龄、体重、食物、肝肾功能、药物代谢酶的基因多态性、疾病因素等)作为协变量因素纳入分析,以识别变异的来源和程度,减少不可解释的变异。对于具有临床意义的影响因素,需进行剂量调整。
PopPK模型由2个部分组成,固定效应和随机效应。固定效应指的是PK参数的典型值及协变量等固定效应的群体估计。随机效应指的是未知的因素导致的模型误差,包括参数随机效应(η)和观测值随机效应(ε)。
02 PopPK分析方法
PopPK的分析方法包括简单数据法NPD(Naïve Pooled Data Analysis)、两步法STS(Standard Two Stage Analysis)、非线性混合效应模型法NONMEM(Nonlinear Mixed Effects Model)等。NPD: 每个时间点的浓度求均值,然后计算均值的参数。STS:第一步先计算各个 人的药代参数,第二步对药代参数进行分析。NONMEM:使用ELS和不同的估计 方法(FO,FOCE,POSTHOC等)估计固定和随机效应参数。
03 PopPK在新药研发中的应用
①PopPK在临床前研究中的应用
临床前PK研究的目的是将临床前动物实验获得的PK结果进行外推,实现人体PK参数的预测,为首次给药剂量提供参考。张澍等人[1]以紫杉醇为例,采用NONMEM 法进行模型拟合,得出二室模型描述紫杉醇在人、大鼠和小鼠的药动学行为较为合理。并通过正态化预测分布误差法对最终模型结果进行评估, 结果准确可靠。通过使用相关生长规律法对最终模型参数进行计算,种属间清除率和总表观分布容积均有相关性。因此该模型方法可以对紫杉醇结构相似药物种属外推和剂量确定过程提供定量依据,为新药研发提供帮助。
②PopPK 在I期临床试验中的应用
I期临床试验是探究人体对药物反应和耐受性,探索药物的安全有效剂量,同时对药物动力学进行研究,为II期临床试验的给药方案提供依据。近年来,在I期临床试验中使用PopPK的研究越来越多,可探究如性别、体重等因素对PK的影响,提供I期研究效率,为Ⅱ 期临床给药提供指导。Kuester等人[2]通过建立PopPK,分析马妥珠单抗(一种人源化抗EGFR单克隆抗体,可以阻断EGFR激活和下游信号的传导,抑制肿瘤生长)I期临床数据,结果表明体重影响中央室表观分布容积和清除率, 提示II期进行剂量选择的时候,应考虑体重的影响。
③PopPK 在II期临床试验中的应用
II期临床试验属于概念验证研究,初步确定药物的安全性和有效性。PopPK可对II期数据进行定量地模型化评估,指导后续III期临床剂量选择。Dosne等人[3]对厄达替尼(一种泛成纤维细胞生长因子受体FGFR抑制剂,具有潜在的抗肿瘤活性)在I期和II期研究(健康志愿者3项,癌症患者3项)收集的数据,进行PopPK分析发现:性别和肾功能是清除率的重要协变量,而体重、性别和α-酸性糖蛋白对中央室表观分布容积有显著影响(图1)。年龄、种族和轻度肝损伤不是影响厄达替尼的显著协变量。PopPK结果将有助于后续药代学/药效学分析和模拟,可以用来支持后期临床试验阶段剂量选择。
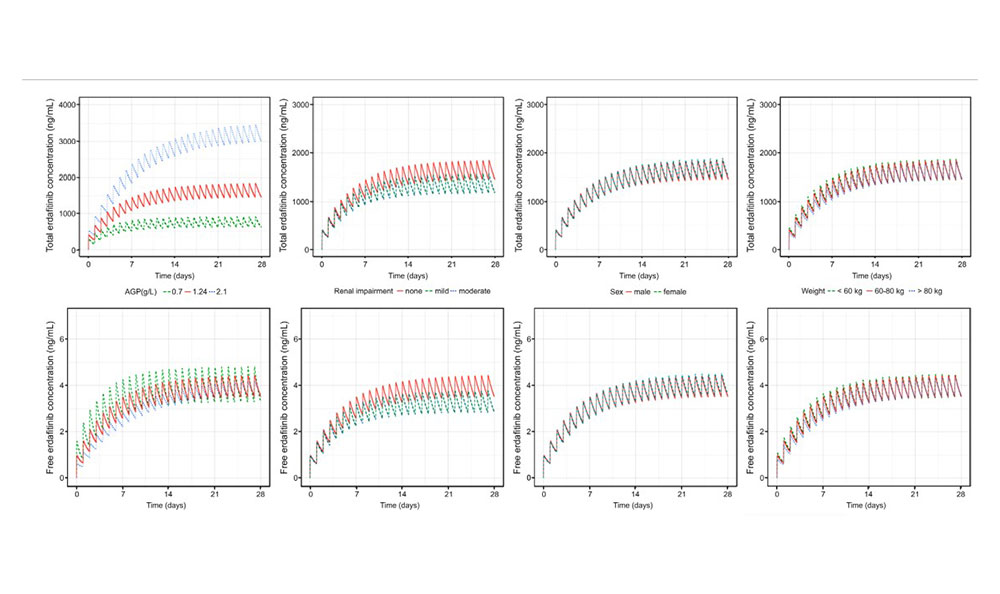
图1. 模拟不同协变量的典型受试者的厄达替尼稳态浓度-时间曲线[3]
④PopPK 在III期和IV期临床试验中的应用
III期临床试验是以较大患者人群为研究对象,进一步对药物的安全性、有效性和不良反应进行评估。IV期临床试验是新药上市后的应用研究阶段,评价在特殊患者人群中的受益和风险关系, 改进给药剂量。III期临床试验阶段,PopPK的主要用途之一是确定协变量对人体药代动力学的影响,对潜在剂量调整和药物说明书至关重要[4]。
此外,PopPK在考察药物与药物相互作用过程、儿科用药等过程起着十分重要的作用。PopPK在药物研发中应用广泛,可以降低试验的盲目性,优化试验方案,缩短新药研发周期,提高研发成功率。
参考文献:
[1]张澍, 任宇鹏, 尚德为,等. 紫杉醇种属间药动学相关性的荟萃分析[J]. 中国药学杂志, 2013, 048(007):546-552.
[2]Kuester K, Kovar A, Lüpfert C, Brockhaus B, Kloft C. Population pharmacokinetic data analysis of three phase I studies of matuzumab, a humanised anti-EGFR monoclonal antibody in clinical cancer development. Br J Cancer. 2008 Mar 11;98(5):900-6. doi: 10.1038/sj.bjc.6604265. Epub 2008 Mar 4. PMID: 18319714; PMCID: PMC2266843.
[3]Dosne AG, Valade E, Stuyckens K, Li LY, Ouellet D, Perez-Ruixo JJ. Population Pharmacokinetics of Total and Free Erdafitinib in Adult Healthy Volunteers and Cancer Patients: Analysis of Phase 1 and Phase 2 Studies. J Clin Pharmacol. 2020 Apr;60(4):515-527. doi: 10.1002/jcph.1547. Epub 2019 Nov 19. PMID: 31742712.
[4]Hu, C., J. Zhang, and H. Zhou, Confirmatory analysis for phase III population pharmacokinetics. Pharm Stat, 2011. 10(1): p. 14-26.